O almacenamento de hidróxeno: as pilas de combustible

A diferenza fundamental entre as pilas de combustible e as baterías convencionais que utilizamos, por exemplo, nos
nosos reprodutores de música é que estas últimas almacenan enerxía química que converten
en electricidade, e unha vez esgotada a pila queda inutilizada ou pode recargarse, se é o caso, enchufando o cargador
á corrente eléctrica. As pilas de combustible non almacenan enerxía química, senón que
producen electricidade a partir da enerxía química dun combustible que se lle proporciona dunha fonte externa.
Polo tanto, seguirán xerando electricidade na medida en que sexan alimentadas de combustible e oxidante.
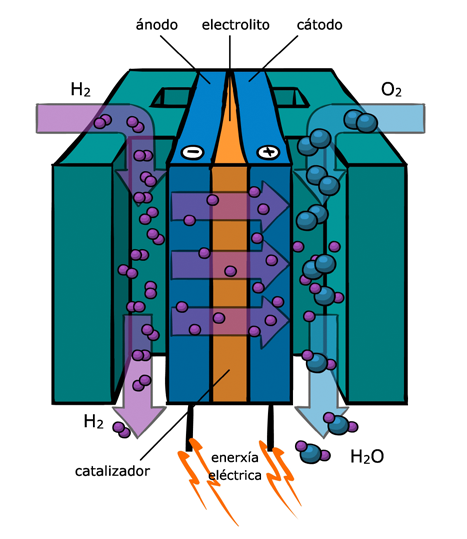
Os reactivos que se utilizan son, por un lado, o hidróxeno (no ánodo), e como oxidante, no lado do
cátodo, o osíxeno. Entre ambos aparece un electrólito ou unha membrana semipermeable que
permitiría o paso dos átomos de hidróxeno do ánodo ao cátodo. Os electróns
liberados na reacción química que rompe o átomo de hidróxeno en protóns e electróns
saen por un circuíto externo como corrente eléctrica. Os electróns volven ao cátodo onde
reaccionan co osíxeno e cos ións de hidróxeno xerando auga como residuo.